宋霞 ,鱼丽莉 ,赵慧 (.兰州大学第二医院药剂科,兰州 730030;
.兰州大学第二医院肿瘤内科,兰州 730030)
免疫检查点抑制剂(immune checkpoint inhibitors,ICIs)能增强人体自身T淋巴细胞的特异性识别及杀伤肿瘤细胞能力,在晚期实体肿瘤及转移性肿瘤治疗中的疗效得到了广泛肯定。但由于其独特的作用机制,ICIs在增强免疫能力的同时也会累及机体正常组织,导致正常的免疫耐受缺失,从而诱发自身免疫样炎症反应,即免疫相关副反应(immune-related adverse events,irAEs)。皮肤免疫相关不良反应(cutaneous immune-related adverse events,cirAE)是ICIs最常见的不良反应,发生率高达30%~50%,且严重程度各不相同,包括斑丘疹、荨麻疹、多形红斑、银屑病、白癜风等,甚至还有可危及生命的中毒性表皮松解坏死症等[1-2]。cirAE可能因患者而异,早期识别和及时干预可降低发病率并减少潜在的肿瘤治疗中断。临床药师作为个体化用药的参与者和药学监护的实施者,可在cirAE的处置中发挥积极作用。本文报道了临床药师参与的1例在我院接受纳武利尤单抗治疗后发生棘皮瘤的胃癌患者的诊治过程。
患者为男性,65岁,2021年7月因间断上腹痛在外院甲行胸腹CT、胃镜及病理检查,确诊为胃基底细胞样鳞状细胞癌,并肝内多发转移。2021年8月,患者在外院乙行骨扫描示多发骨转移,遂行2周期晚期一线治疗,具体方案为:白蛋白紫杉醇 180 mg,d1,8+顺铂 40 mg,d1~3+纳武利尤单抗360 mg,d1。2021年9月,患者于我院肿瘤内科就诊,排除化疗禁忌后于2021年9月19日至2022年1月24日行第3~7周期化疗,具体方案同前。患者肿瘤控制可,疗效评价为部分缓解。2022年2月28日至4月19日,患者于我院继续接受第8~10次免疫维持治疗,具体方案为:纳武利尤单抗360 mg,d1,每3周1次。5月9日,患者因右手背皮肤结节于我院整形外科门诊行右侧手背部结节活检术。5月16日,患者为行第11次免疫治疗入我院,自诉胸背部结节样病变瘙痒难忍。临床药师详细问诊,患者入院查体示体温36.5 ℃、心率82次/min、呼吸16次/min、血压132/70 mmHg(1 mmHg=0.133 kPa),全身散在结节化病变(直径1~2 cm),部分表面破溃结痂;
实验室检查提示Ⅰ度骨髓抑制,肿瘤标志物较前下降,结合胸腹部CT评价为肿瘤稳定。5月9日的右手背皮肤组织活检病理回报皮肤中央鳞状上皮增生向间质内生长,周围大量炎症细胞浸润,考虑棘皮瘤,各切缘干净。患者自述自外院乙首次输注纳武利尤单抗约15 d后,头皮出现多处散在性瘙痒丘疹,触摸疼痛,且在随后的半个月发展为角化过度的结节(直径0.5~1.0 cm,图1A),胸部前侧和背部出现新的病变。患者自行使用卤米松乳膏,但症状未见改善。因瘙痒难忍,患者抓挠斑块致结节破裂,后每天自行局部使用云南白药膏加碘伏涂抹治疗后,结节表面塌陷,结痂成棕色斑块。考虑到当时肿瘤疗效评价为疾病缓解,故医师允其继续使用纳武利尤单抗,同时开具夫西地酸钠软膏和炉甘石洗剂交替使用。经对症处理后,患者皮损保持稳定。然而,在第9次使用纳武利尤单抗后的体格检查中医师发现,患者颈部周围多发圆顶状丘疹和结节,有或无角化过度。在随后的2周内,病灶自上而下迅速扩散,患者躯干、下肢和脚底角化结节较多,手背侧角化丘疹和斑块超过20个(图1)。在完成10次治疗后,患者又出现口腔溃疡伴黏膜红肿,经皮肤科及口腔科会诊,明确为皮肤棘皮瘤及口腔扁平苔藓。
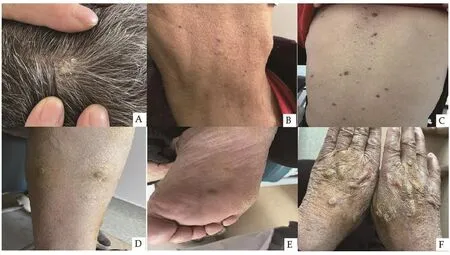
图1 患者棘皮瘤临床表现(2022年5月16日)
针对上述病史,临床药师与医师联合查阅相关文献,通过对该类不良事件的临床发生特点、高危因素、治疗手段及预后进行综合判定,最终认为患者的棘皮瘤与纳武利尤单抗有关,遂嘱患者口服维A酸胶囊40 mg,每天2次+依巴斯汀片10 mg,每天1次,同时予卤米松乳膏外涂,暂不停止免疫治疗。5月18日,患者再次(第11次)接受免疫维持治疗,予纳武利尤单抗注射液360 mg,静脉滴注。患者自诉脚趾在自行进行的中药药浴期间有疼痛,查体可见脚趾上有红肿紫绀,医师与药师协商后予患者口服塞来昔布胶囊0.2 g,每天1次镇痛。5月21日,患者自诉瘙痒明显改善,可忍受,但脚趾疼痛感仍存在,临床药师嘱患者穿棉质袜子及宽松鞋子,带维A酸胶囊、依巴斯汀片、卤米松乳膏出院治疗。
出院1周后药师电话随访,患者诉棘皮瘤暂时稳定,脚趾无疼痛,但口腔症状改善不明显。6月9日,患者接受第12次免疫治疗。6月11日,临床药师电话随访,患者自诉自用药结束后,颈部及手背部发痒并出现若干小丘疹。7月4日,患者入院行第13次免疫治疗,自诉近期乏力、困倦明显,棘皮瘤进展,查体可见其颈部新发数个圆顶状丘疹,手部结节样斑块连接成片,手臂及下肢均有新病灶出现。患者甲状腺功能检查示三碘甲状腺原氨酸0.01 nmol/L、甲状腺素0.01 nmol/L、游离三碘甲状腺原氨酸1.29 pmol/L、游离甲状腺素1.46 pmol/L、促甲状腺激素142.8 μIU/mL,行甲状腺功能抗体三项、甲状腺彩超及垂体前叶素检查,排除垂体、肾上腺等腺体破坏,考虑纳武利尤单抗致甲状腺功能减退,请内分泌科医师会诊后决定予患者左甲状腺素钠片。对于患者是否可以再次使用纳武利尤单抗这一问题,医师与临床药师进行了详细讨论;
同时,对患者进行PHQ-9抑郁症筛查量表评分,判定其处于中度抑郁。考虑到患者已进入纳武利尤单抗赠药阶段,且只剩最后2剂,加之患者的抗肿瘤治疗愿望较为强烈,基于最大获益和尊重患者意愿,医师和临床药师均同意患者继续使用纳武利尤单抗,同时对其进行积极的心理疏导。8月18日,患者接受最后1次纳武利尤单抗治疗。9月8日药师随访,患者手背棘皮瘤有所消退,腿部及脚底无新增病变(图2)。
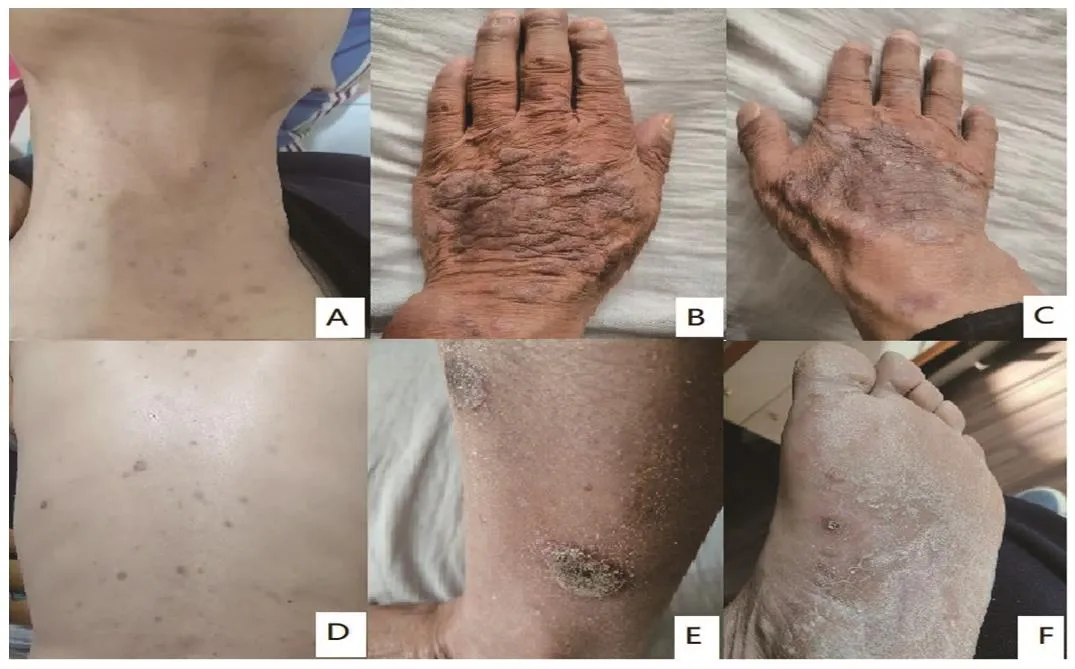
图2 患者棘皮瘤临床表现(2022年9月8日)
2.1 患者棘皮瘤与纳武利尤单抗的关联性评价
棘皮瘤在接受ICIs治疗的病例报道中相对罕见。该病起源于皮肤和黏膜的皮脂腺滤泡,通常表现为坚硬的锥形结节,中心可见鳞片状堵塞[3]。ICIs致棘皮瘤的病理生理机制尚未明确,但学者普遍认为是T细胞介导的:cirAE的发展涉及ICIs对肿瘤细胞和真皮-表皮交界处和/或皮肤的其他部位共表达抗原的阻断,ICIs可通过重新激活CD4+/CD8+T细胞来靶向皮肤真皮/表皮的抗原,并在与正常皮肤发生交叉反应后诱发炎症反应[4]。棘皮瘤的形成涉及多种因素,包括遗传易感性、DNA损伤、炎症、局部或全身免疫改变等[5]。目前,已有报道指出,维罗非尼、索拉非尼、芦可替尼、来氟米特、维莫德吉等多种药物均可引发棘皮瘤[5-6]。
对于本例患者而言,判定引发棘皮瘤的原因是明确治疗方案的第一步。临床药师依据《药品不良反应报告和监测管理办法》[7]推荐的因果关系评价方法对该患者棘皮瘤与纳武利尤单抗之间的关联性判定为“肯定”。理由如下:(1)该患者发生棘皮瘤与纳武利尤单抗免疫治疗有合理的时间关系;
(2)纳武利尤单抗药品说明书中的不良反应虽未提及棘皮瘤,但是国外文献[8]已有报道;
(3)该患者既往无皮肤病史,无细菌真菌感染,不存在可引起棘皮瘤的其他相关危险因素(如紫外线长期照射、吸烟、其他化学致癌物和创伤);
(4)再次用药期间,该患者棘皮瘤处于发展中,符合“再激发阳性”;
(5)该患者既往合并使用的其他治疗药物如白蛋白紫杉醇及顺铂均无此类不良反应报道。综上,临床药师判定该患者的棘皮瘤与免疫治疗直接相关。
2.2 患者确诊为棘皮瘤后的治疗方案选择分析
临床药师查阅了美国临床肿瘤学会的《ICIs治疗的患者免疫相关不良事件处理实践指南》、美国国家综合癌症网络指南《免疫治疗相关毒性的管理》以及中国临床肿瘤协会(Chinese Society of Clinical Oncology,CSCO)的《ICIs相关的毒性管理指南》,均未直接发现ICIs相关棘皮瘤的具体处置措施。我国《皮肤鳞状细胞癌诊疗专家共识(2021)》提到,角化棘皮瘤是皮肤鳞状细胞癌的特殊亚型,手术切除是治疗的常规治疗方法,但主要针对孤立性病灶。其他非手术治疗方式包括:(1)局部药物治疗,如联合外用氟尿嘧啶和咪喹莫特乳膏;
(2)冷冻疗法和电干燥刮除术,用于具有多个病灶、边界清晰的皮损;
(3)光动力疗法;
(4)放射治疗;
(5)系统治疗,包括使用化疗药物(维A酸类药物)、免疫及靶向治疗等[9]。考虑到ICIs相关毒性反应的特殊性,为了清晰地了解ICIs相关棘皮瘤的临床特征、治疗方案及转归,临床药师进一步查阅了国内外报道的相关病例报道,并对其进行了总结[5,8,10-18],详见表 1。
由表1可见,在检索到的16例相关病例中:(1)男女发病比例为1.29∶1,且年龄均大于60岁;
(2)原发肿瘤以黑色素瘤多见(6例,37.50%);
(3)棘皮瘤发病潜伏期长短不一,介于1.4~18个月;
(4)累及部位主要包括躯干及四肢;
(5)棘皮瘤的处置手段包括停药(5例,31.25%)、切除/冷冻手术/电干燥刮除术(6例,37.50%)、局部应用强效激素(6例,37.50%)、病灶内注射曲安奈德等激素(5例,31.25%)等;
(6)暂无死亡病例,所有患者均预后良好,其中8例(50.00%)患者可继续使用ICIs,不良反应转归时间介于2周~1年。
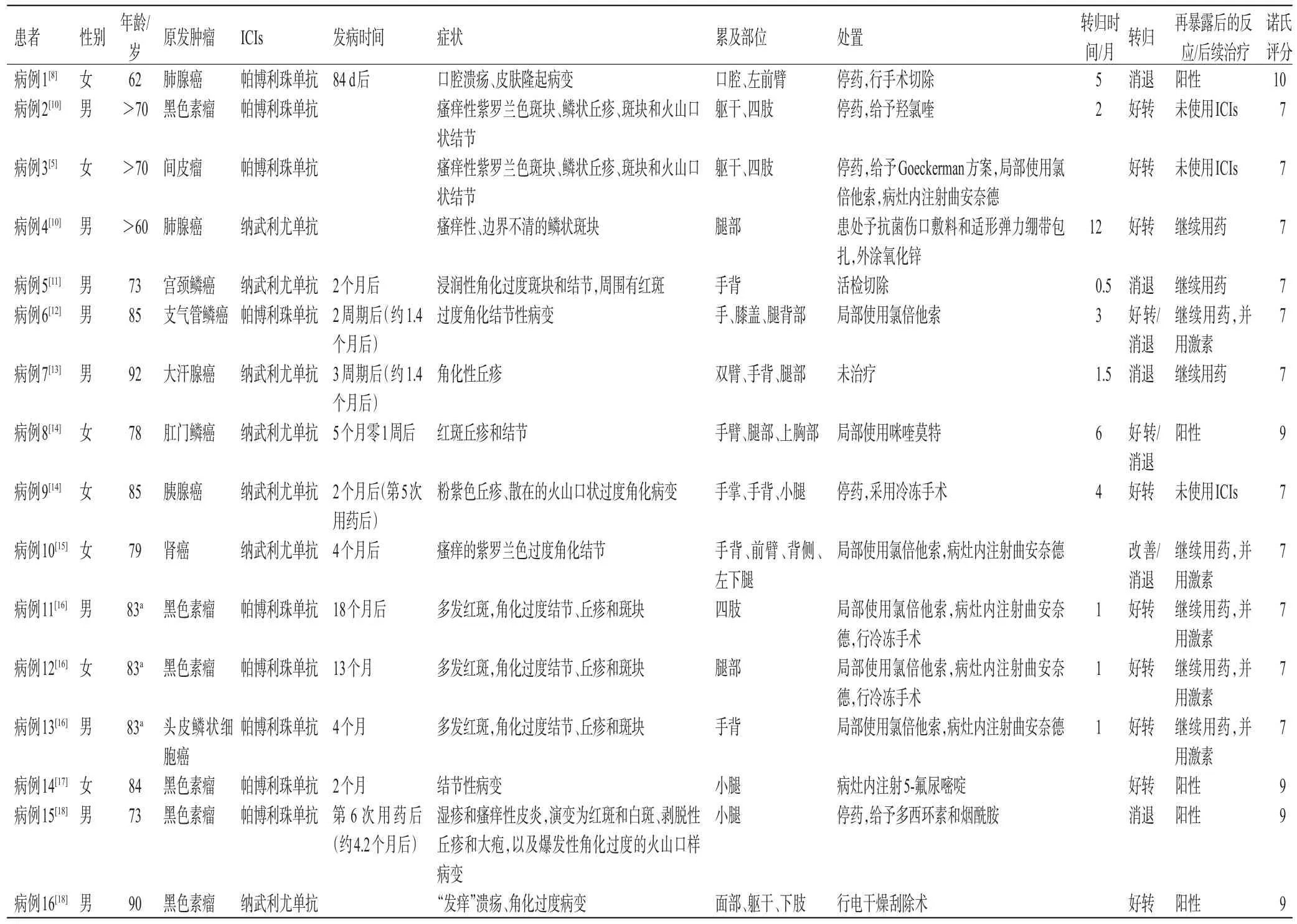
表1 文献报道的16例免疫检查点抑制剂相关棘皮瘤患者临床资料
本例患者为63岁的男性,其棘皮瘤累及头皮、颈部、躯干、手臂、手背、腿部及脚底,与上述病例特征基本相符。该患者在用药后2周发病,潜伏期短于上述病例。首先,该患者的棘皮瘤泛发于全身多个部位,不具备单个手术切除的条件;
其次,由于经济原因,该患者拒绝激光及冷冻治疗;
最后,病灶内注射曲安奈德可能存在影响血糖的潜在风险,由于病灶数繁多,该患者治疗意愿不佳。与此同时,该患者的棘皮瘤还伴发瘙痒。CSCO的《ICIs相关的毒性管理指南》将瘙痒症分为轻、中、重3个等级,该患者伴有强烈且广泛的瘙痒,呈间歇性,因挠抓致皮肤受损,属于中度,推荐可在加强止痒治疗(如局部使用强效糖皮质激素+口服抗组胺药)的情况下继续使用ICIs。综合以上因素,在考虑药物有效性、安全性、经济性、可及性的总体原则下,以控制瘙痒及稳定皮肤病变为目的,临床药师与医师讨论后最终决定予该患者强效卤米松乳膏外用+维A酸胶囊口服+依巴斯汀片口服的综合治疗方案。
2.3 关于继续用药后棘皮瘤持续恶化的治疗决策干预
该患者确诊为棘皮瘤后,先后于5月18日、6月9日分别接受1剂纳武利尤单抗治疗,在前述对症方案治疗的基础上,棘皮瘤进一步加重,全身多个部位出现新发病变,手背病变迅速融合。7月4日,患者再次入院,医师查体明确棘皮瘤处于进展中,对于此时是否需要停用免疫治疗,临床药师从有效性、安全性、经济性3个角度进行了分析:(1)有效性方面,患者为胃癌多发肿瘤,在使用纳武利尤单抗治疗期间,原发疾病控制可,抗肿瘤疗效评价为疾病缓解,免疫治疗获益肯定。(2)安全性方面,从棘皮瘤的发生发展过程可知,随着纳武利尤单抗用药次数或者累积剂量的增加,不良反应持续进展,且该患者处于精神过度紧张的状态,日常生活明显受到该不良反应干扰,不愿交流、外出,心情低落,睡眠欠佳,注意力难以集中,PHQ-9抑郁症筛查量表评分为12分,可能存在中度忧郁。(3)经济性方面,该患者目前处于纳武利尤单抗的患者援助赠药阶段,经济负担不重。
基于以上三点,医师与临床药师分别从疾病及药物治疗的角度与患者进行了沟通,阐明当前治疗困局及获益-风险情况,患者表示对肿瘤治疗仍有坚定的信心,且该药物赠药还有最后2剂,故选择继续用药,待免疫治疗结束后再考虑对棘皮瘤患处进行对症干预。研究指出,棘皮瘤发展具有典型的3个阶段:(1)增殖阶段,快速发病并扩大,可持续2~4周;
(2)成熟阶段,表现为典型的带有角质核心的圆顶状结节;
(3)回归阶段,角质栓塞消退和破裂,形成色素减退的瘢痕[19]。考虑到目前患者瘙痒已得到控制,棘皮瘤主要累及感官不适但并未危及生命,加之该病发病具有自限性,故临床药师和医师在最大程度尊重患者意愿的前提下,同意其继续治疗,并嘱其动态关注病情变化。除此之外,临床药师还制定了详细的用药教育清单、皮肤护理注意事项清单、用药监护及随访计划等,并积极对患者进行心理疏导,在后续使用纳武利尤单抗治疗的每个周期评估患者的不良反应控制情况,观察其皮肤结节是否坍塌、消退或保持稳定,瘙痒症状是否反复,已有棘皮瘤病灶是否进一步扩大,患者身体其他部位是否爆发新的丘疹或结节等。最终该患者如期完成免疫治疗;
同时,在暴露因素消除20 d后的随访中,其棘皮瘤已经呈现消退的态势。
cirAE往往是ICIs较为常见也较早发生的不良反应,其临床表现多样,多数损伤轻微可逆,仅有少数可致患者永久停药甚至死亡。目前,ICIs致棘皮瘤仅在帕博利珠单抗和纳武利尤单抗中有所报道。该类不良反应预后良好,治疗效果明显,早期识别和干预可防止病变恶化,并能避免治疗中断。ICIs致棘皮瘤可能对患者的社会功能及生活质量产生不利影响,因此适当的皮肤护理和心理干预是必需的。在确认本例患者发生棘皮瘤后,临床药师发挥专业所长,与医师通力协作,专业互补,在不良反应原因鉴别、治疗方案筛选等方面给出了建设性的意见,最大限度地尊重了患者的治疗意愿并保护了患者的权益,体现了临床药师在治疗团队中的价值。
猜你喜欢 免疫治疗单抗药师 药师“归一”中国医院院长(2022年21期)2022-11-30FOLFOXIRI联合贝伐单抗±阿替利珠单抗治疗转移性结直肠癌实用肿瘤学杂志(2022年3期)2022-11-30医院静配中心曲妥珠单抗剩余液信息化管理与成效医院管理论坛(2022年7期)2022-10-14药师带您揭开华法林的面纱保健医苑(2022年4期)2022-05-05肿瘤免疫治疗发现新潜在靶点中国生殖健康(2020年7期)2020-12-10司库奇尤单抗注射液皮肤性病诊疗学杂志(2020年4期)2020-09-02癌症免疫治疗相关的PD1-PDL1通路作用机制及其研究进展天津医科大学学报(2019年3期)2019-08-13使用抗CD41单抗制备ITP小鼠的研究中国卫生标准管理(2015年16期)2016-01-20暴发型流行性脑脊髓膜炎早期诊断及免疫治疗探讨中外医疗(2015年18期)2016-01-04非小细胞肺癌免疫治疗临床新进展医学研究杂志(2015年5期)2015-06-10